
[h=2]

دما: تغییرات دما حتما روی انحلال پذیری مواد جامد، مایع و گاز تأثیر می گذارد. البته این اثرات فقط به طور محدود برای گازها و جامدات تعیین شده اند.
[h=2]مواد جامد: اثر دما روی مواد جامد، بسته به این که واکنش گرماگیر است یا گرمازا، فرق می کند. با استفاده از اصل لوشاتلیه می توانیم اثر دما روی هر دو واکنش را معین کنیم.
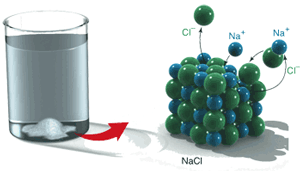
در واکنش گرمازا (که گرما به قسمت محصولات واکنش که همان یون های تجزیه شده مواد جامد واکنش دهنده هستند، اعمال می شود)، افزایش دما در قسمت محصولات، یک تغییر در حالت تعادلی واکنش ایجاد می کند، طبق اصل لوشاتلیه واکنش به سمت واکنش دهنده ها پیش می رود. با این جابجایی و تعادل جدید، مقدار کمی از مواد جامد واکنش دهنده تجزیه می شوند و انحلال پذیری کاهش پیدا می کند.
[h=2]مایعات: تغییرات دما، هیچ رفتار مشخصی روی انحلال پذیری مایعات ندارد. شاید هیچ گاه ترکیب حلال – حل شونده ای که هر دو به صورت مایع هستند، با مشکل مواجه نشود.
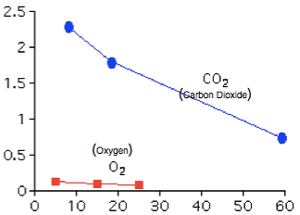
[h=2]گازها: در مورد مواد، نخست به یاد داشته باشد که دما، مقیاس و میزانی از انرژی جنبشی متوسط ماده را نشان می دهد. وقتی دما افزایش پیدا می کند، حرکت مولکول های گاز بیش تر شده و بنابراین احتمال این که ذرات گاز حل شده در مایع، به فاز گازی فرار کنند بیش تر می شود و ذرات گاز موجود، کم تر حل می شوند.
|
بنابراین افزایش دما به معنای انحلال پذیری کم تر و کاهش دما به معنای انحلال پذیری بیش تر برای گازهاست.
طبق اصل لوشاتلیه، این رفتار گازها را بهتر می توان فهمید. ابتدا دقت کنید که حل شدن گاز در مایع معمولا گرمازا است؛ بنابراین افزایش دمای اعمال شده به سمت محصولات این واکنش، یک تغییر در سیستم به وجود می آورد. پس سیستم به سمت واکنش دهنده ها پیش می رود تا این تغییر را کم تر کند. در نتیجه، غلظت تعادلی ذرات گاز در فاز گازی افزایش پیدا خواهد کرد و انحلال پذیری گاز، کم تر خواهد شد. برعکس این حالت نیز برای کاهش دما در سمت محصولات برای گاز اتفاق می افتد. یعنی کاهش دما طبق اصل لوشاتلیه باعث افزایش انحلال پذیری گاز می شود.
[h=2]

فشار: اثر فشار بر روی انحلال پذیری مواد جامد و مایع بسیار کوچک است؛ بنابراین از اثر فشار بر روی گازها صحبت خواهیم کرد:
در مورد گازها با ترکیب اصل لوشاتلیه و قانون هنری می توان اثر فشار را روی انحلال پذیری آن ها بررسی کرد. قانون هنری بیان می کند هنگامی که دما ثابت است، انحلال پذیری گاز با فشار جزئی آن متناسب است:
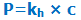
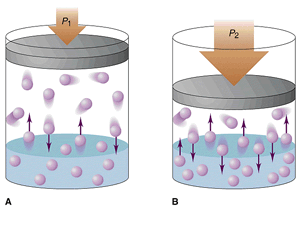
سیستمی را در نظر بگیرید که در آن مقداری گاز در مایع حل شده است. افزایش فشار باعث افزایش فشار جزئی (فشار وارد بر هر قسمت از این ترکیب) می شود و گاز بیش تر متراکم می شود. افزایش فشار جزئی به این معناست که ذرات گازی بیش تری وارد مایع می شوند (گاز بالای مایع در این حالت، کم تر می شود) و فشار جزئی نیز با این تغییر، کاهش پیدا می کند؛ یعنی برای کم کردن اثر این تغییر در افزایش فشار، واکنش خود را به گونه ای تغییر می دهد که انحلال پذیری بیش تر شود.
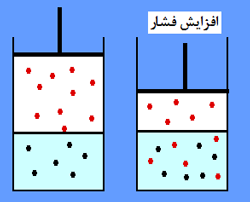
|
اگر در همین حالت، فشار وارد بر سیستم را کاهش می دادیم، مولکول های گازی بیش تری از مایع فرار می کردند و برای همین انحلال پذیری کم تر می شد.

برای فهم مطالب بالا بهتر است این واکنش تعادلی را با هم بررسی کنیم:
انحلال پذیری دی اکسید کربن با تغییرات زیر چه تغییری می کند؟
الف) دما افزایش پیدا کند.
ب) فشار و دما افزایش پیدا کنند.
ج) فشار، افزایش ولی دما کاهش پیدا کند.
د) فشار کاهش پیدا کند.
جواب:
الف) واکنش گرما زا است؛ بنابراین افزایش در دما به معنای کاهش انحلال پذیری است.
ب) افزایش در هر دو عامل فشار و دما در این واکنش به معنای انحلال پذیری بیش تر است.
ج) با اطلاعات داده شده، نمی توان فهمید انحلال پذیری چه تغییری می کند.
د) افزایش در فشار، باعث وارد شدن مولکول های گازی بیش تری به مایع می شود تا فشار جزئی را کاهش دهد؛ بنابراین انحلال پذیری افزایش پیدا می کند.

