پیوند پای
اوربیتالهای مولکولی حاصل از ترکیب اوربیتالهای اتمی (2P)، کمی پیچیدهاند. سه اوربیتال (2P) هر اتم، در امتداد محورهای مختصات دکارتی (X ، Y ، Z ) قرار دارند. اگر تشکیل یک مولکول دو اتمی را از طریق نزدیک شدن اتم ها در امتداد یکی از این محورها مثلاً (X) در نظر بگیریم، دو اوربیتال اتمی (P[SUB]x[/SUB]) سر به سر به یکدیگر نزدیک میشوند و در نتیجه همپوشانی، دو اوربیتال مولکولی پیوندی
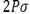
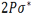
تعریف پیوند پی
پیوند کووالانسی که تراکم الکترونی آن در دو ناحیه بالا و پایین محور متصل کننده دو اتم پیوند بیشتر است، پیوند پی (
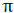
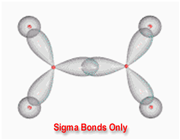
اوربیتال پیوندی مولکولی پی (
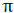
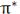
در تشکیل یک مولکول دو اتمی، دو اوربیتال اتمی (P[SUB]z[/SUB]) از پهلو به هم نزدیک میشوند و دو اوربیتال مولکولی، یکی اوربیتال پیوندی پی (
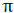
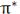
اوربیتالهای
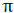
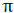
در هر حال اثر نهایی اوربیتال
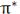
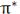
اوربیتالهای اتمی (P[SUB]y[/SUB]) نیز از پهلو به هم نزدیک میشوند. این دو اوربیتال اتمی نیز یک مجموعه ی دوتایی اوربیتال مولکولی
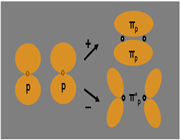
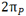
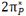
دو اوربیتال
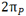
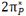
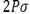
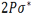
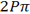
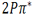
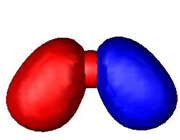
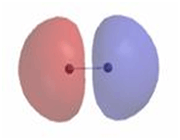
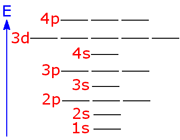
انرژی یک اوربیتال مولکولی به موارد زیر بستگی دارد:
1. انرژی اوربیتالهای اتمی تشکیل دهنده آن
2. میزان و نوع همپوشانی اوربیتالهای اتمی در هنگام تشکیل آن
مقایسه انرژی
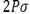
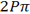
چون میزان همپوشانی اوربیتالهای 2P در تشکیل اوربیتال مولکولی 2P[SUB]6[/SUB] بیشتر از همپوشانی آن ها برای به وجود آوردن اوربیتال مولکولی
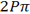
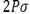
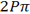
مرکز یادگیری تبیان - تهیه و تنظیم: فاطمه گودرزی
